Deux temps forts de sensibilisation ont lieu conjointement sur la même semaine : la semaine nationale de lutte contre le cancer et la semaine du cerveau. Ces deux évènements clés sont l’occasion de partager la mobilisation d’Imagine for Margo sur les cancers du cerveau de l’enfant, de l’adolescent et du jeune adulte et de rappeler l’importance de faire avancer la recherche sur ces cancers, tumeurs les plus fréquentes et dont les formes les plus graves sont particulièrement difficiles à soigner.
Le combat d’Imagine for Margo contre les cancers du cerveau de l’enfant, de l’adolescent et du jeune adulte
Plus qu’un combat, une urgence ! Les tumeurs cérébrales sont la première cause de décès par cancer chez les enfants, les adolescents et les jeunes adultes et sont malheureusement fréquentes en oncologie pédiatrique. En effet, ces pathologies constituent la deuxième forme de cancer la plus fréquente en pédiatrie, après les leucémies (environ 30 % des cancers pédiatriques, dans le monde). L’incidence et la mortalité associées à ces tumeurs varient selon les régions et les types spécifiques de tumeurs. En France, environ 500 nouveaux cas de tumeurs cérébrales sont diagnostiqués chaque année chez les enfants et les adolescents (3 000 en Europe). Ces tumeurs sont responsables de près de 30 % des décès liés au cancer dans cette tranche d’âge.
Les tumeurs cérébrales pédiatriques regroupent un ensemble de cancers du système nerveux central aux caractéristiques très variées. Elles peuvent être bénignes ou malignes, infiltrantes ou bien délimitées, et toucher différentes structures du cerveau et de la moelle épinière. Les principaux types de tumeurs cérébrales pédiatriques sont :
- Les gliomes de la ligne médiane
Les gliomes de la ligne médiane, incluant les gliomes infiltrants du tronc cérébral, sont des tumeurs agressives. Ils représentent environ 10 à 20 % des tumeurs cérébrales pédiatriques. Ces tumeurs touchent principalement les enfants âgés de 5 à 10 ans. Le pronostic est sombre, avec une survie médiane inférieure à un an. En savoir plus sur les gliomes de l’enfant
- Les médulloblastomes
Le médulloblastome est la tumeur cérébrale maligne la plus courante chez l’enfant, représentant environ 20 % des tumeurs cérébrales pédiatriques. L’incidence est estimée à 1 cas pour 200 000 enfants par an. Le taux de survie à cinq ans varie entre 60 et 70 %, en fonction des sous-types moléculaires et des facteurs de risque.
- Les tumeurs rhabdoïdes
Les tumeurs tératoïdes rhabdoïdes atypiques (ATRT) sont des tumeurs rares et agressives, représentant environ 1 à 2 % des tumeurs cérébrales pédiatriques. Elles surviennent principalement chez les enfants de moins de 3 ans. Le pronostic est réservé, avec un taux de survie à cinq ans inférieur à 50 %.
- Les épendymomes
L’épendymome est la troisième tumeur cérébrale maligne la plus fréquente chez l’enfant. Près de 1000 nouveaux cas d’épendymome pédiatrique sont diagnostiqués en Europe chaque année. Ces tumeurs sont plus fréquentes chez les enfants âgés de moins de 5 ans.
Des traitements pour lutter contre les tumeurs du cerveau encore insuffisants
Les tumeurs cérébrales pédiatriques sont traitées par une combinaison de méthodes thérapeutiques, chacune ayant ses spécificités et limitations.
- Chirurgie :
La résection chirurgicale est souvent le premier traitement envisagé pour les tumeurs cérébrales de l’enfant. Elle vise à enlever la tumeur autant que possible sans endommager les tissus cérébraux sains, ce qui peut être très complexe. Cependant, certaines tumeurs sont situées dans des zones difficiles d’accès ou proches de structures vitales, rendant l’exérèse impossible, comme pour le gliome infiltrant du tronc cérébral.
- Radiothérapie :
La radiothérapie utilise des rayonnements toxiques pour détruire les cellules tumorales. Elle est fréquemment employée en complément de la chirurgie ou lorsque celle-ci n’est pas envisageable. Néanmoins, chez les enfants de moins de 3 ans, la radiothérapie est utilisée avec prudence en raison des risques d’effets secondaires sur le développement cérébral.
- Chimiothérapie :
La chimiothérapie consiste à administrer des médicaments pour éliminer les cellules cancéreuses. Elle est parfois utilisée en association avec la chirurgie et la radiothérapie. Cependant, l’efficacité de la chimiothérapie peut varier selon le type de tumeur, et les effets secondaires, en particulier sur la moelle osseuse, doivent être surveillés attentivement. Par ailleurs, la barrière hémato-encéphalique est un frein majeur, qui se heurte au déploiement de la chimiothérapie pour les tumeurs cérébrales. Cette barrière étanche, qui entoure les vaisseaux sanguins cérébraux, empêche l’entrée d’un grand nombre de molécules dans le cerveau.
Il est essentiel de noter que le choix du traitement dépend de nombreux facteurs, notamment le type de tumeur, de sa localisation, de l’âge de l’enfant et de son état de santé. Malgré les avancées thérapeutiques, certaines tumeurs restent difficiles à traiter, soulignant la nécessité de poursuivre la recherche pour accélérer le développement de thérapies efficaces et peu toxiques.
En effet, les traitements des tumeurs du cerveau chez l’enfant, l’adolescent et le jeune adulte peuvent entraîner des effets secondaires tardifs, qui apparaissent parfois immédiatement après la fin des soins, mais aussi après plusieurs mois ou années. Ces séquelles varient en fonction du type de tumeur, des traitements reçus et de l’âge du patient au moment de sa prise en charge. Parmi les complications possibles, des troubles hormonaux peuvent survenir lorsque la radiothérapie affecte l’hypophyse ou l’hypothalamus, entraînant notamment un ralentissement de la croissance. Les fonctions cognitives peuvent également être impactées, en particulier chez les jeunes enfants traités par radiothérapie, provoquant des difficultés d’apprentissage, de mémoire et de concentration. D’autres séquelles incluent des troubles sensoriels, comme une altération de la vision ou de l’audition, des problèmes de croissance et de développement, des troubles neurologiques tels que des convulsions ou des problèmes de coordination, ainsi qu’un risque accru de développer un second cancer. Face à ces enjeux, un suivi médical à long terme est essentiel pour assurer une prise en charge adaptée et pour améliorer la qualité de vie des patients guéris.
Un héritage laissé par Margo pour poursuivre son combat
En 2011, Margo, 14 ans, est emportée par une tumeur cérébrale agressive contre laquelle les pédiatres oncologues étaient démunis. Pas d’essai clinique, pas de traitement efficace. Pour lutter contre cette injustice, Margo a initié une collecte de fonds en ligne pendant sa maladie pour financer la recherche sur son type de cancer du cerveau, avec le rêve de faire progresser nos connaissances et les traitements. Ainsi, plus de 100 000 euros ont été remis au Dr. Jacques Grill et son équipe de recherche à Gustave Roussy. Après son décès, ses parents, Olivier, notre trésorier, et Patricia, notre présidente, ont trouvé 3 mots dans l’un de ses carnets : Go, Fight, Win. Un message d’espoir qu’Imagine for Margo adresse aux familles du monde touchés par ce fléau :
- « Go » vas-y : saisis les opportunités qui se présentent, ne manque pas une chance de réaliser tes rêves.
- « Fight » bas-toi contre tous les moments difficiles qui t’arriveront.
- « Win » gagne et accomplis les choses que tu veux, réalise tes rêves et essaye toujours d’être une personne meilleure.
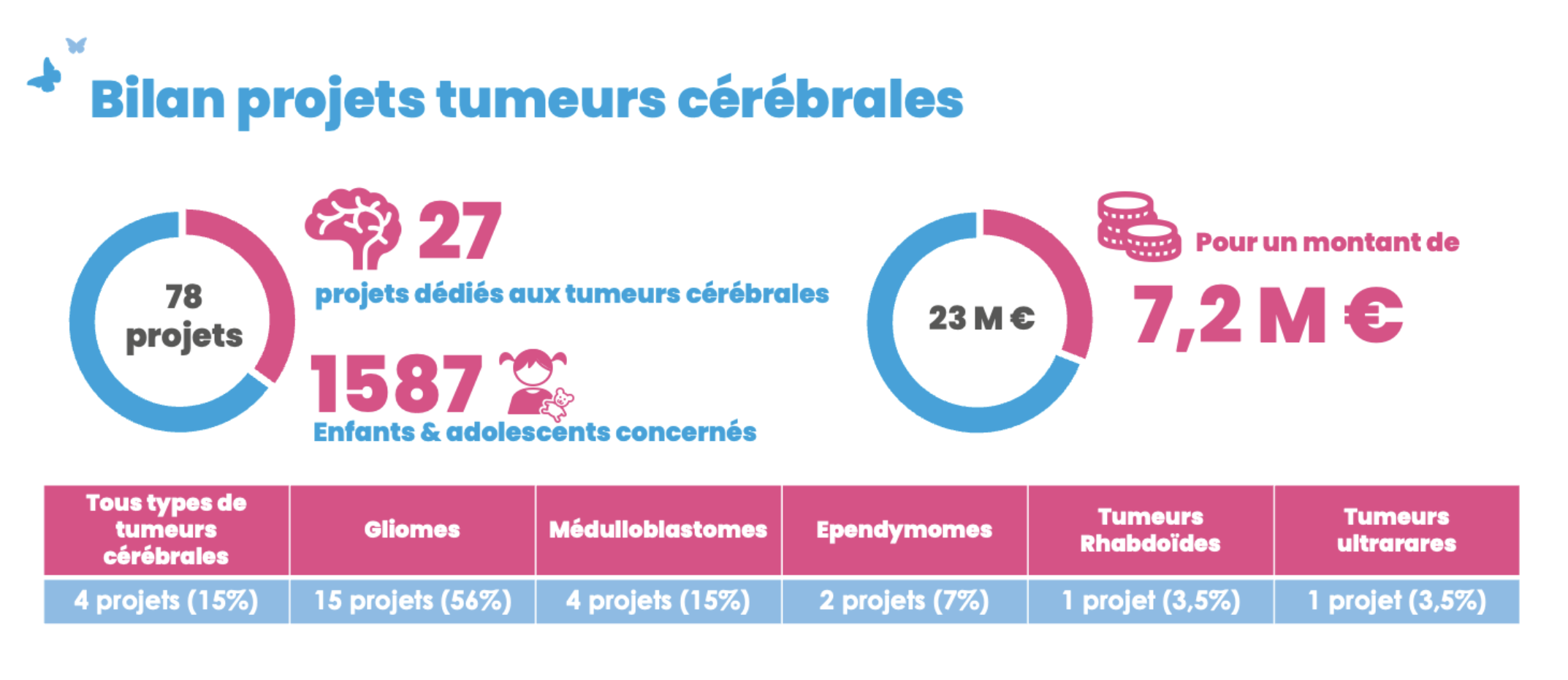
L’héritage de Margo constitue les solides fondations de notre association et le combat que nous menons : accélérer les innovations pour tous les enfants, adolescents et jeunes adultes atteints d’un cancer, avec pour objectif de les guérir plus et de les guérir mieux. D’années en années, nos records de collecte se sont accumulés grâce à la mobilisation et à la générosité de nos donateurs, collecteurs et partenaires. Ainsi, depuis 2011, nous avons pu financer 78 projets de recherche à hauteur de 23 millions d’euros. Tous les projets de recherche que nous finançons ont été sélectionnés pour leur excellence, leur innovation et leur impact pour les patients, par des comités d’experts internationaux. Parmi eux, 27 programmes sont dédiés à améliorer les innovations thérapeutiques dans les tumeurs cérébrales de l’enfant, ce qui représente, 7,2 millions d’euros.
Ces projets visent bien entendu à financer des essais cliniques, étape essentielle de soin permettant de valider les traitements de demain. Cependant, il n’y a pas d’innovation si nous n’apportons pas notre soutien aux projets de recherche en amont, qui permettent de faire naître des innovations. Ainsi, nous finançons des projets de recherche translationnelle de thérapie ciblée ou d’immunothérapie, convaincus que ces dernières sauront réussir là où les traitements actuels échouent. Enfin, nous soutenons également les équipes de recherche qui tentent de limiter les séquelles des tumeurs et des traitements. En 2024, nous avons financé 8 programmes de recherche européens dédiés aux tumeurs cérébrales, via notre appel à projets FIGHT KIDS CANCER, dont « REVIIH-BT ». Ce projet, piloté par le Dr Michael Reber et la Pr Natacha Entz-Werlé, offre aux enfants des solutions permettant de compenser des pertes d’acuité visuelle. Ce projet de téléréhabilitation visuelle sera proposé à 100 enfants, adolescents et jeunes adultes et s’effectuera à l’hôpital et à domicile, à travers des exercices réalisés par réalité virtuelle. Des résultats préliminaires à cette étude viennent d’être publiés dans le journal Lancet et indiquent que neuf participants sur dix ont montré une amélioration cliniquement significative de la fonction visuelle et/ou de la vision fonctionnelle, notamment la restauration du champ visuel binoculaire et l’augmentation de la vitesse de lecture. Ces effets positifs ont été maintenus lors du suivi à 6 mois
Explorer les tumeurs du cerveau jusqu’à l’infiniment petit
L’exploration de la génétique, notamment à travers l’analyse de toutes les modifications génétiques de l’ADN de la tumeur ainsi que de l’ADN tumoral circulant (ADNtc), offre des perspectives prometteuses pour le diagnostic, le pronostic et le suivi des tumeurs cérébrales pédiatriques. Le projet de plateforme de diagnostic moléculaire de la Dr Pascale Varlet (APHP) a utilisé un grand éventail de techniques moléculaires de pointe afin de mieux classifier les tumeurs cérébrales et de créer un référentiel nouveau, favorisant la médecine personnalisée. Grâce à ce travail, de nombreux patients ont bénéficié de ce savoir nouveau, ce qui a permis de leur rendre un diagnostic plus précis. De plus, avec l’essor chaque jour plus important de ces techniques d’exploration génétique, Imagine for Margo a décidé, en 2025, de soutenir le programme du Dr Claire Pecqueur (Université de Nantes), dans le cadre des Rallyes du Cœur. Ce projet explorera la diversité des gliomes pédiatriques de haut-grade ainsi que leur capacité à s’adapter aux traitements. Ces tumeurs, au pronostic sombre, présentent des états moléculaires et cellulaires similaires à ceux observés dans les tumeurs adultes. L’étude se basera sur 20 modèles cellulaires de gliomes de haut-grade pédiatriques et emploiera des techniques d’exploration moléculaire avancées. En obtenant une image plus claire de la variabilité et de l’évolution de ces maladies, il sera dès lors possible d’espérer des traitements plus efficaces et personnalisés, améliorant ainsi les chances de survie des enfants atteints de ce cancer difficile.
Les analyses de l’ADN tumoral circulant (ADNtc) peuvent également se révéler déterminantes pour mieux guérir les enfants. Ces fragments d’ADN, issus de la tumeur principale et présents dans les fluides corporels (sang, urine, liquide céphalo-rachidien), reflètent les altérations génétiques des tumeurs et peuvent être détectés par des prélèvements non invasifs, tels que des prises de sang. Cette approche permet de suivre l’évolution des tumeurs, d’identifier de nouvelles mutations associées aux rechutes et d’évaluer la réponse aux traitements. Par exemple, des études ont démontré la faisabilité d’effectuer un profil génomique tumoral à partir de l’ADNtc chez de jeunes patients atteints de neuroblastome, avec une concordance de 97 % avec les analyses classiques sur les prélèvements tumoraux. Pour aller plus loin dans ce sens, en 2024, nous avons décidé d’apporter, via FIGHT KIDS CANCER, notre soutien au projet « SOUP ». Les nombreuses équipes impliquées dans ce projet effectueront les analyses génétiques de l’ADNtc de plus de 500 patients, ce qui permettra de mieux suivre l’évolution de leur tumeur cérébrale et de mieux adapter, le cas échéant, les traitements.
Des modèles d’étude fiables pour innover contre le médulloblastome
Le médulloblastome est la plus fréquente des tumeurs embryonnaires du système nerveux central. Cette pathologie se développe dans le cervelet, qui est important dans le contrôle moteur ou l’équilibre et est également impliqué dans certaines fonctions cognitives comme l’attention ou l’apprentissage spatial. Le médulloblastome est une tumeur maligne qui a l’aspect d’un tissu embryonnaire et est est une forme de cancer invasive. Au moment du diagnostic, près de la moitié des enfants présentent des métastases qui sont rarement symptomatiques. La majorité de ces tumeurs survient avant l’âge de 10 ans (40% avant 5 ans et 75% avant 10 ans) mais certaines peuvent également affectées des adolescents et de jeunes adultes. Le traitement est décidé selon le groupe de risque (de 1 à 4), de la possibilité d’une intervention chirurgicale, de la présence de métastases et de facteurs biologiques marqueurs de la sévérité de la tumeur. Concernant les patients à haut-risque, le pronostic s’est nettement amélioré avec des stratégies thérapeutiques comportant plusieurs cures de chimiothérapie à haute-dose et de radiothérapie. Cependant, leur marge de progression reste encore importante, notamment grâce à l’essor de la médecine de précision, de l’immunothérapie et l’apparition de nouveaux modèles d’étude fiables de la maladie, notamment pour les groupes 3 et 4, les plus agressifs. À ce propos, le projet « FIGHT4MB », que nous avons sélectionné en 2024 via FIGHT KIDS CANCER, s’attèle à développer un modèle in vivo pour le groupe 4. Cette forme est aussi malheureusement la plus difficile à guérir puisque 40% des patients rechutent après le traitement standard, et la rechute est systématiquement fatale. Afin de mieux comprendre la maladie et de pouvoir tester de nouvelles thérapies curatives, les chercheurs impliqués dans ce projet ambitieux réaliseront des modèles in vitro et in vivo, en se basant sur les découvertes des cellules à l’origine de la maladie et les altérations génétiques responsables. Ces modèles seront validés puis seront amenés à être rapidement déployés à l’ensemble de la communauté scientifique internationale.
Fort heureusement, il existe des modèles pour le groupe 3, sur lesquels le Dr Célio Pouponnot de l’Institut Curie travaille et dont nous finançons les projets. Ses recherches lui permettent de tester de nouvelles approches thérapeutiques dans les projets MEDULLODRUGS (FIGHT KIDS CANCER, 2023) et RADIOMEDSCREEN (FIGHT KIDS CANCER, 2024). « Pour mener des études sur le médulloblastome de groupe 3, on disposait déjà de plusieurs modèles cellulaires et des modèles in vivo, dans lesquels on implantait des cellules tumorales de patients. Ces modèles restent malgré tout limités. Récemment, nous avons réussi à générer des modèles de « mini-cerveaux », ou organoïdes, de médulloblastome de groupe 3. Pour se faire, on conçoit des organoïdes du cervelet à partir de cellules souches, dans lesquelles nous insérons les gènes altérés, responsables de la maladie. C’est un modèle qui reflète l’état des cellules au moment de la formation du cervelet chez l’embryon, où apparaît des cellules qui sont à l’origine de la tumeur. Nous utilisons également des organoïdes tumoraux, réalisés à partir d’échantillons de patients. Ces deux modèles nous permettent d’étudier la sensibilité des cellules de médulloblastome de groupe 3 à plusieurs traitements, à la fois à un stade précoce et à un stade où la maladie est installée. » Dr Célio Pouponnot
L’autre avantage de cette technologie est la possibilité de pouvoir en générer plusieurs milliers rapidement et ainsi tester des milliers de médicaments. Ainsi pour ces deux projets, il est possible de cribler des centaines de molécules, principalement des médicaments hors indication, en combinaison avec la radiothérapie pour ce qui est du projet RADIOMEDSCREEN. Le but de ces projets est de trouver de nouvelles molécules plus à même de lutter efficacement contre le médulloblastome, tout en minimisant l’impact des traitements. « Pour déterminer si un médicament candidat est d’intérêt pour le traitement de la maladie, nous mesurons le niveau de mort cellulaire, ce qu’on appelle l’apoptose. Nous pouvons également voir si le traitement provoque un blocage du cycle cellulaire, soit stopper la progression de la prolifération des cellules de medulloblastomes. Nous pouvons également, pour les traitements les plus intéressants, étudier leur mécanisme d’action au sein de la cellule tumorale. Ces études doivent obligatoirement être poursuivies in vivo, pour voir l’efficacité et la toxicité de la molécule, une étape indispensable. »
Même si le développement de thérapies ciblées est une évidence, l’immunothérapie doit également être explorée pour le traitement du médulloblastome de groupe 3. Le projet CARBEMED (FIGHT KIDS CANCER, 2021) vise à développer une immunothérapie innovante contre ces tumeurs qui affaiblissent le système immunitaire du patient. Ces tumeurs sont caractérisées par l’amplification de l’oncogène MYC, qui favorise un microenvironnement tumoral immunosuppresseur, notamment via la voie du TGF-β, une cytokine impliquée dans la croissance tumorale et l’inhibition de la réponse immunitaire. L’équipe de recherche a identifié B7H3, comme une cible antigénique prometteuse, présente sur les cellules tumorales mais absente des tissus sains. Le projet explore l’utilisation des cellules T-CAR, qui consiste en une transformation génétique de lymphocytes anti-tumoraux afin de les forcer à reconnaître la cible B7H3. De plus, les cellules T-CAR anti-B7H3 ont été également modifiées pour résister à l’inhibition du TGF-β, afin de renforcer son action contre la tumeur. À ce stade, les chercheurs ont généré les cellules T-CAR anti-B7H3 et ont réalisé dans un premier temps des tests in vitro qui se sont révélés positifs. Ils ont également réalisé des premières études in vivo, qui ont montré que ces cellules thérapeutiques s’attaquaient très rapidement, et avec une grande efficacité, à des médulloblastomes qui avaient été préalablement implantés. Ces résultats, très encourageants, sont encore préliminaires et doivent être encore confirmés.
Des traitements épigénétiques contre les tumeurs rhabdoïdes
Les tumeurs rhabdoïdes sont des cancers rares mais très agressifs qui affectent notamment les jeunes nourrissons et les enfants de moins de 3 ans. Ce type de cancer peut se développer dans de multiples organes, dont le cerveau, et les traitements prescrits combinent chirurgie, radiothérapie et chimiothérapie. Cette approche thérapeutique n’est efficace que pour une minorité de patients, qui, de plus, souffriront d’importantes séquelles. Il est donc nécessaire de développer des traitements efficaces ciblant les particularités moléculaires et génétiques. De récents travaux ont montré que 95 % des tumeurs rhabdoïdes sont liées à une altération du gène SMARCB1, censé empêcher la prolifération cellulaire. Cette mutation génétique peut être héréditaire (mutation germinale) ou uniquement survenir dans les cellules tumorales, comme cela est souvent le cas.
L’équipe du Dr Franck Bourdeaut à l’Institut Curie est depuis 2020 en charge du projet « EpiRT » qui vise à développer une approche par épigénétique pour lutter contre ce cancer. L’épigénétique est une branche de la biologie qui étudie comment l’expression de nos gènes peut être modifiée sans altérer la séquence de l’ADN. En d’autres termes, bien que notre génome reste inchangé, des mécanismes épigénétiques peuvent influencer l’activation ou l’inactivation de certains de ses gènes. Les régulations épigénétiques jouent un rôle essentiel dans le développement et le fonctionnement de notre organisme. Par exemple, elles permettent à des cellules, ayant le même ADN, de se spécialiser en un type cellulaire précis, comme des cellules de la peau, du cœur ou des neurones. De plus, elles peuvent être influencées par des facteurs environnementaux tels que l’alimentation, le stress, les cycles jour/nuit ou l’exposition à des substances chimiques. Comprendre l’épigénétique est crucial, car ces modifications peuvent avoir des implications sur notre santé, influençant le risque de développer certaines maladies, comme des cancers, ou la réponse à des traitements. « Les tumeurs rhabdoïdes ne présentent pas de mutation autre que SMARCB1, qui est un acteur épigénétique majeur. Les effets de la perte de SMARCB1 correspondent à une vaste désorganisation épigénétique. Nous testons donc des traitements épigénétiques tentant de rétablir certains de ces déséquilibres ». Dr Franck Bourdeaut
Ces découvertes sont relativement récentes en biologie et nous assistons, de plus en plus, à l’émergence de thérapies épigénétiques en santé. Ce projet vise donc à développer des « epidrugs » qui vont cibler l’action de SMARCB1 altérée, comme les inhibiteurs EZH2 ou DNMT qui ont montré des signaux d’efficacité, mais transitoires, dans les tumeurs rhabdoïdes. Ces inhibiteurs ont donc été testés en combinaison avec d’autres traitements sur des modèles de tumeurs rhabdoïdes, en laboratoire. Parmi les molécules testées, la combinaison de 2 agents (dont le nom reste confidentiel) a montré des effets importants pour bloquer l’évolution tumorale de tumeurs humaines dans un modèle murin. Des études complémentaires d’évolution du profil génétique des tumeurs traitées ont été lancées afin de mieux comprendre le mécanisme thérapeutique, qui a des chances d’être développé en clinique. Ces nouveaux traitements sont très prometteurs, en particulier pour des tumeurs dont le profil génétique est trop altéré. Par ailleurs, leur toxicité semble être faible, ce qui est une bonne nouvelle mais qu’il faut néanmoins nuancer comme le précise le Dr Franck Bourdeaut : « La plupart des médicaments épigénétiques ont peu d’effets secondaires à court terme. En revanche, leur utilisation chez de jeunes enfants, chez qui les mécanismes épigénétiques sont déterminants pour le bon développement de leur organisme, incitent à une prudence concernant les effets à long terme, en particulier sur le cerveau chez des petits nourrissons. »
Guérir enfin du Gliome Infiltrant du Tronc Cérébral, un cancer du cerveau jusque-là incurable
Les gliomes proviennent ainsi de cellules support des neurones, à savoir les astrocytes ou les oligodendrocytes. Ces tumeurs, très fréquentes parmi les tumeurs pédiatriques, sont de différents grades : gliome de bas grade, gliome anaplasique et glioblastome (qui regroupe notamment les gliomes de la ligne médiane ou les gliomes infiltrants du tronc cérébral). Pour ces formes de haut-grade, nos connaissances ont considérablement progressé ces dernières années, notamment grâce au projet BIOMEDE que nous avons très fortement soutenu. Nous savons à présent que les gliomes malins de l’enfant ne ressemblent pas du tout aux formes adultes et cette distinction doit maintenant guider les stratégies thérapeutiques à venir. Des mutations très particulières de gènes, jamais décrites dans un autre cancer, régulant l’organisation de l’ADN et son expression ont été récemment décrites dans ces tumeurs.
Le gliome infiltrant du tronc cérébral ainsi que celui de la ligne médiane sont traités de manière différente des autres gliomes malins. Leur localisation dans des régions critiques du cerveau, comme le tronc cérébral et leur caractère infiltrant rendent difficile voire impossible toute tentative chirurgicale. Elles sont biopsiées afin d’affirmer le diagnostic, de réaliser le profil moléculaire de la tumeur et ainsi donner au patient les traitements les plus adaptés. De plus, la radiothérapie est systématiquement utilisée à la dose maximale possible (55-60 Gy) et se limite, en général, au volume tumoral. Malheureusement, peu de chimiothérapies ont une efficacité reconnue dans les gliomes de haut-grade. Les enfants sont alors le plus souvent traités dans le cadre d’essais cliniques ou bénéficient de traitements expérimentaux dans le cadre d’un accès précoce ou compassionnel.
Depuis plus de 10 ans, nous soutenons le combat que mène le Dr Jacques Grill contre les gliomes de l’enfant à Gustave Roussy. Après avoir financé un premier essai, VINILO, Imagine for Margo a apporté un soutien de 1,6 millions d’euros au Dr Jacques Grill pour réaliser la plus grande étude clinique au monde sur le Gliome Infiltrant du Tronc Cérébral : BIOMEDE. Cette tumeur cérébrale maligne est très agressive et est localisée dans une zone vitale du tronc cérébral, appelée le pons. Cette région cérébrale contrôle des fonctions vitales comme l’équilibre, la respiration, la fréquence cardiaque ou la tension artérielle et est également traversée par les nerfs contrôlant la vision, l’audition, la parole, la déglutition et le mouvement.
Les premières victoires contre le Gliome Infiltrant du Tronc Cérébrale grâce à BIOMEDE 1
Conduit entre 2014 et 2019, la première phase de BIOMEDE a permis de démontrer l’utilité de la biopsie au diagnostic comme un standard, permettant ainsi d’effectuer le profilage moléculaire systématique des tumeurs de chaque enfant afin de mieux connaître la maladie. « Quand on a lancé BIOMEDE, nous ignorions que la cause de cette maladie reposait sur une mutation dans un gène, celui de l’histone H3. Ce gène produit une protéine qui sert à empaqueter l’ADN. À cause de cette mutation, la cellule ne va pas arriver à se différencier, c’est-à-dire à devenir un neurone ou un astrocyte. Cette cellule va persister dans son état de cellule souche, avec toutes ses caractéristiques, et notamment sa mobilité et sa résistance aux traitements. » Dr Jacques Grill – interview complète à retrouver en cliquant ici.
En fonction des résultats, le Dr Jacques Grill et son équipe ont comparé l’efficacité de 3 médicaments (erlotinib, dasatinib et évérolimus), associés à des séances de radiothérapie. Cette première phase a impliqué 70 centres localisés dans 9 pays européens, en Australie et en Nouvelle-Zélande et a inclus 233 patients. Le profil de toxicité et la légère amélioration de la médiane de survie globale obtenus au cours l’étude ont permis de retenir l’évérolimus, comme traitement de référence pour la seconde partie de l’essai, BIOMEDE 2. Ce traitement a permis notamment, pour la première fois au monde, de sauver les 4 premiers enfants de ce cancer.
« Il y a plusieurs enfants qui sont très longs survivants, c’est à dire qui ont une survie supérieure à 3 ans après le diagnostic. De plus, 4 enfants sont guéris dont Lucas, qui est l’enfant qui a la survie la plus longue, puisqu’il a été diagnostiqué il y’a plus de 7 ans. Pour tous ces patients, l’évérolimus, en plus des séances de radiothérapie, était le traitement qui leur fallait. On continue à les surveiller tous les trois mois et on cherche également les explications de leur longévité. On sait déjà qu’ils n’ont pas tous les mêmes mutations que Lucas. Nous avons un article sous presse qui analyse justement ces patients. » précise le Dr Jacques Grill.
Par ailleurs, le profilage moléculaire des tumeurs prélevées par biopsie ont permis de faire des analyses des mutations associées au degré de gravité de ces gliomes, et ce notamment grâce à l’utilisation de l’Intelligence Artificielle (BIOMEDE IA). Par conséquent, au terme de ce projet, et en plus de BIOMEDE 2, des projets de recherche voient le jour grâce au soutien que nous apportons aux essais PATOI ou encore aux projets du Dr David Castel et du Dr Béatrice Rondinelli, afin de trouver des thérapies correspondants encore plus aux altérations moléculaires identifiées dans BIOMEDE 1.
BIOMEDE 2 : accélérer la guérison du Gliome Infiltrant du Tronc Cérébral
Cet essai, ouvert depuis le 23 septembre 2022, consiste à comparer l’effet thérapeutique de l’ONC 201 à l’évérolimus, le traitement de référence, toujours en association la radiothérapie. Ouvert dans 10 pays européens (40 centres), cet essai prévoit d’inclure 368 patients adultes et enfants en 4 ans. L’ONC 201 est le premier médicament d’une nouvelle classe d’anticancéreux, qui cible le métabolisme énergétique des cellules cancéreuses et a montré, aux Etats-Unis, des signaux d’efficacité chez certains patients en rechute d’une tumeur cérébrale maligne de la ligne médiane. Cette efficacité est due à la présence d’une mutation au sein de la tumeur, H3K27M, qui sera détectée grâce à un séquençage de la tumeur à partir d’une biopsie.
« Si aujourd’hui je peux dire que l’évérolimus est un très bon médicament pour certains types de patients, c’est grâce à la force de BIOMEDE. Aucun industriel ne se serait d’ailleurs lancé dans un essai comme ça. Cet essai s’est fait grâce à l’aide d’organismes comme l’Institut national du cancer et Imagine for Margo et qui va maintenant, je l’espère, inspirer d’autres équipes. » Dr Jacques Grill
Aller encore plus loin pour lutter contre les Gliomes de Haut-Grade grâce à l’immunothérapie
L’immunothérapie est une approche thérapeutique innovante qui vise à stimuler le système immunitaire du patient pour qu’il reconnaisse et attaque les cellules cancéreuses. Contrairement aux traitements conventionnels comme la chimiothérapie ou la radiothérapie, qui ciblent directement les cellules tumorales, l’immunothérapie renforce les défenses naturelles de l’organisme pour lutter contre le cancer. Il existe plusieurs types d’immunothérapies, notamment les anticorps monoclonaux, qui bloquent des mécanismes inhibiteurs du système immunitaire, les inhibiteurs de points de contrôle immunitaire, qui réactivent les lymphocytes T contre la tumeur, ou encore les cellules CAR-T, qui sont des cellules immunitaires modifiées génétiquement pour reconnaître et détruire spécifiquement certaines cellules cancéreuses. Ces thérapies ont montré des résultats prometteurs dans plusieurs cancers, notamment les leucémies ou les lymphomes (NIVO-ALCL, GLO-BNHL), et commencent à être explorées pour les tumeurs solides.
Néanmoins, pour les tumeurs solides pédiatriques, et notamment du cerveau, l’immunothérapie se heurte à des difficultés. Le projet de recherche « MiMic Kids » (FIGHT KIDS CANCER 2024), vise à améliorer la compréhension et le traitement des gliomes de haut-grade pédiatriques, en s’appuyant sur des modèles précliniques innovants, de « mini-cerveau ». Les thérapies contre les gliomes malins restent limitées en raison d’une mauvaise prise en compte des interactions entre les cellules immunitaires (notamment la microglie et les macrophages) et les cellules tumorales de gliome. L’équipe du Dr Ginhoux a développé des organoïdes neuronaux contenant de la microglie et des macrophages, offrant un modèle plus fidèle d’étude. Ils ont déjà généré des « tumoroïdes » pour six patients et sont déjà à même d’analyser l’impact du microenvironnement immunitaire sur la progression du gliome.
« Il s’agit de comprendre comment les cellules tumorales, saines et immunitaires, interagissent entre elles, comment réveiller une réponse immunitaire contre les cellules cancéreuses et pourquoi le système immunitaire des enfants régule mal le cancer », selon la Dr Claudia Pasqualini, qui fait partie de l’équipe en charge de ce projet à Gustave Roussy.
L’objectif du projet est de tester et de valider de nouvelles immunothérapies sur ces modèles 3D dérivés de patients, avec trois axes principaux : évaluer l’efficacité de traitements immunitaires existants, identifier des biomarqueurs de réponse ou de résistance et tester de nouvelles combinaisons thérapeutiques. L’ambition est de repositionner des médicaments dans des essais pédiatriques en cours (AcSé/eSMART, BIOMEDE, ELICIT) ou d’explorer le développement de nouveaux traitements en partenariat avec des start-ups du Paris Saclay Cancer Cluster.
Nos connaissances dans ce domaine doivent progresser et plusieurs essais utilisant des cellules CAR-T sont actuellement en cours dans le traitement des gliomes pédiatriques de haut-grade, notamment aux Etats-Unis, dont l’équipe du Pr Crystal McKall a apporté la preuve de concept en sauvant un premier enfant, ou en Italie, où l’équipe du Dr Francesca DelBufalo tente de reproduire les résultats qu’ils ont obtenu avec des patients atteints d’un neuroblastome en rechute. Ils avaient démontré que, parmi les 27 patients présentant un neuroblastome en rechute et qui ont reçu leur thérapie CAR-T cell anti-GD2, 17 ont bénéficié d’une réponse thérapeutique, qui fût complète pour 9 d’entre eux.
Depuis 2 ans, Imagine for Margo soutient des projets qui tentent de développer cette technologie porteuse d’espoir en France. C’est le cas du projet du Dr Sophie Fougeray de l’Université de Nantes ou encore de l’essai européen « ELICIT », porté par le Dr Jacques Grill. La plateforme ELICIT a été créée pour accélérer le passage des immunothérapies pédiatriques du stade préclinique à l’application clinique à grande échelle. Son objectif est de produire des données de phase II solides et standardisées, afin de convaincre les régulateurs et l’industrie pharmaceutique de développer ces traitements de manière ambitieuse en pédiatrie. Trois essais cliniques seront développés progressivement au sein de cette plateforme innovante : un premier testant une combinaison de thérapie ciblée et d’inhibiteurs de points de contrôle immunitaire pour stimuler la réponse antitumorale, un deuxième utilisant une virothérapie oncolytique pour rendre les gliomes pédiatriques plus détectables par le système immunitaire, et un troisième explorant la thérapie CAR-T cell pour cibler directement les cellules tumorales. C’est un projet innovant dans lequel nous croyons beaucoup et qui est suffisamment adaptable pour accueillir des projets encore plus innovants, notamment à l’heure où les avancées de l’immunothérapie sont particulièrement spectaculaires en recherche translationnelle.
Ensemble, continuons de gagner des victoires contre les cancers cérébraux pédiatriques
« Le combat contre les cancers du cerveau de l’enfant, de l’adolescent et du jeune adulte est encore loin d’être gagné, mais, grâce à notre mobilisation, nos armes sont nettement plus redoutables qu’il y’a 14 ans » Patricia Blanc, présidente d’Imagine for Margo.
Depuis sa création en 2011, Imagine for Margo est un acteur indispensable et moteur du progrès en oncologie pédiatrique en France et en Europe. Même si cet article n’a mis en lumière qu’une partie des projets focalisés sur la recherche contre les cancers cérébraux pédiatriques, il convient également de rappeler l’importance des grands programmes de séquençages des cancers en rechute (Mappyacts) ou à haut risque (MICCHADO), des essais cliniques innovants comme AcSé-ESMART ou du programme SACHA. Ces programmes ont amélioré nos connaissances d’un grand nombre de cancers pédiatriques cérébraux sur les altérations moléculaires et les médicaments qui peuvent les cibler. Cette approche est également en voie d’être appliquée à grande échelle aux tumeurs cérébrales, à travers le programme de recherche translationnelle européen « ITCC Brain Tap », financé en 2024. Ce projet vise à accélérer le développement de nouveaux traitements pour les tumeurs cérébrales pédiatriques en structurant une approche rigoureuse à trois niveaux. D’abord, les chercheurs travailleront avec les experts de l’ITCC pour établir une cartographie des cibles thérapeutiques les plus prometteuses et la mettre à jour régulièrement afin de prioriser les pistes à explorer. Ensuite, ils mettront en place une chaîne d’expérimentation préclinique efficace, utilisant des modèles tumoraux variés et les infrastructures de la plateforme ITCC-P4, afin de tester rapidement les traitements ciblés. Enfin, des liens étroits seront noués avec le comité des sponsors de l’ITCC pour s’assurer que les cibles les plus pertinentes puissent avancer efficacement vers des essais cliniques, en collaboration avec des équipes d’investigateurs et des entreprises pharmaceutiques. Cette approche structurée et ambitieuse a le potentiel de combler le fossé entre la recherche et l’application clinique, augmentant ainsi le nombre d’essais et accélérant l’accès des jeunes patients à des traitements innovants.
Soutenir Imagine for Margo pour vaincre le cancer des enfants
Si de grandes avancées en cancérologie pédiatrique ont vu le jour ces dernières années, grâce aux projets que nous finançons, c’est parce que la mobilisation autour de notre association grandit de plus en plus chaque année. Nous avons la certitude chez Imagine for Margo que rassembler, fédérer et briser les silos permettront un jour de vaincre les cancers pédiatriques. Ensemble, nous sommes plus forts ! Rejoignez-nous pour offrir un espoir de guérison à chaque enfant, adolescent et jeune adulte.
GO, FIGHT, WIN !